매우 우수한 임상 결과 발표.







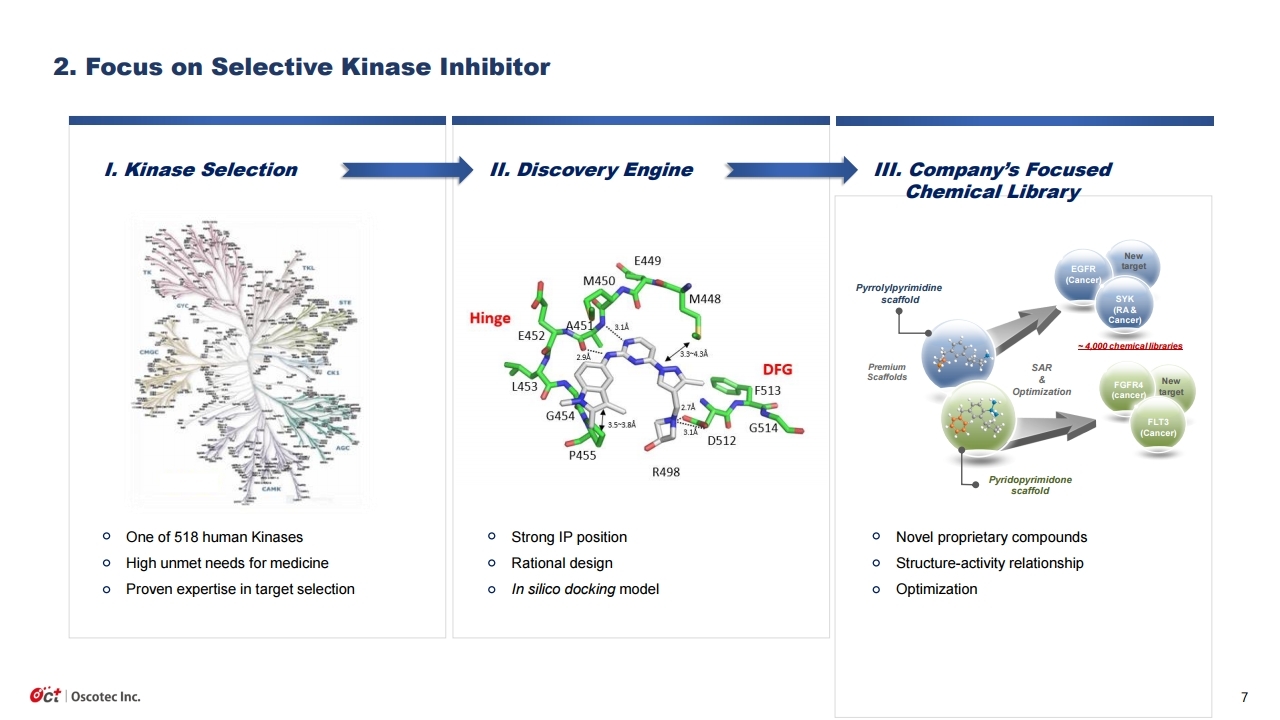



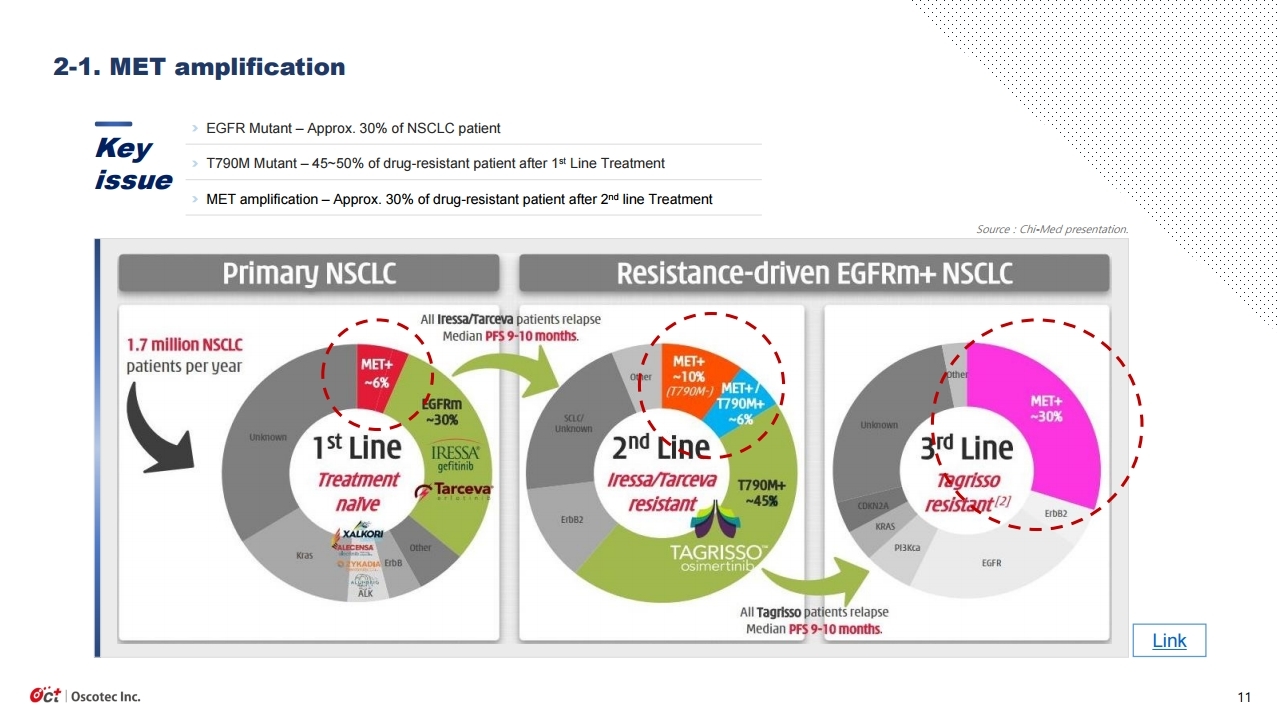













지난 9/20 ESMO에서 동사의 ‘레이저티닙(lazertinib)’과 얀센의 ‘아미반타맙(Amivantamab)’ 병 용요법의 놀라운 임상 1b상 결과가 발표되었다. 해당 결과발표에 대한 기대감으로 주가는 몇일 전 부터 상승세였고, 발표직후 다시한번 급등하였다. 발표내용을 요약하면, 항암제 투여경험이 없는 EGFR 비소세포폐암 환자 20명에게 ‘레이저티닙+아미반타맙’ 병용투여시 100%의 객관적반응률 (ORR)이 나타났고, 타그리소 내성 환자 45명에게도 36%의 객관적반응률이 나타났다. 상당히 우수한 결과이며, 향후 진행될 ‘레이저티닙+아미반타맙’의 글로벌 3상 기대감도 커졌다.
끝이 아니고 시작이다. 연말까지 모멘텀이 쌓여 있다.
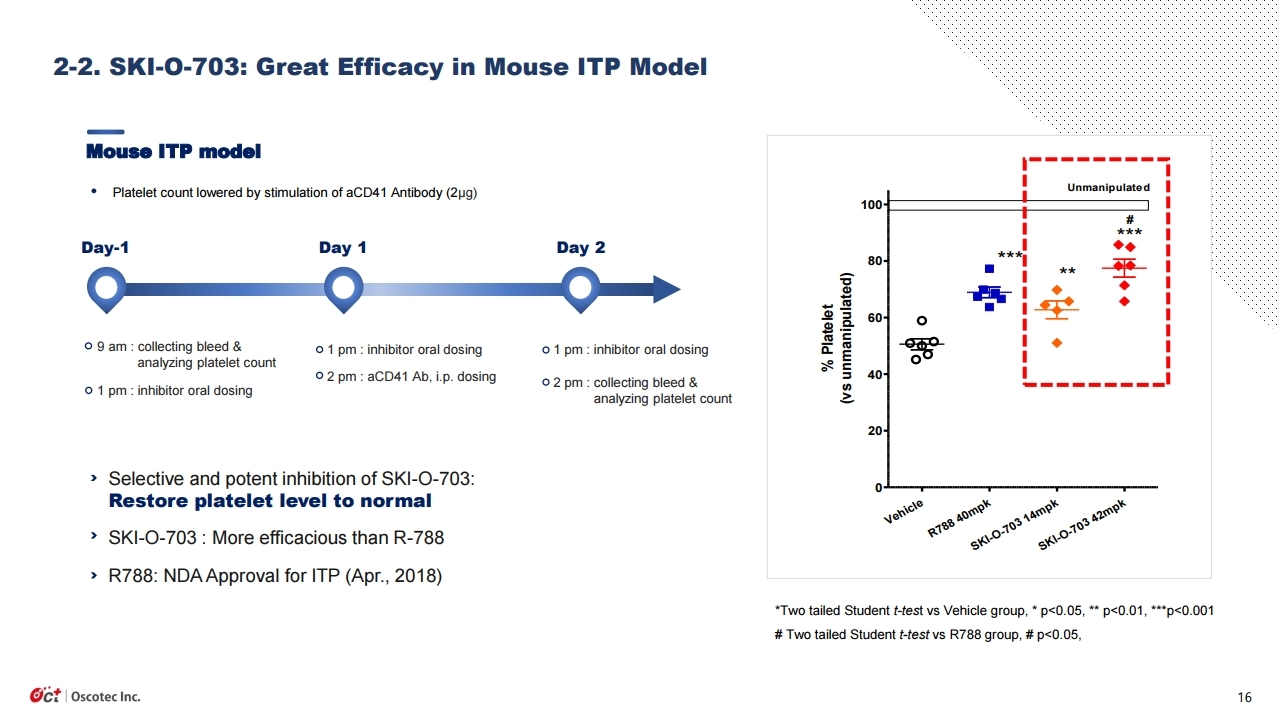
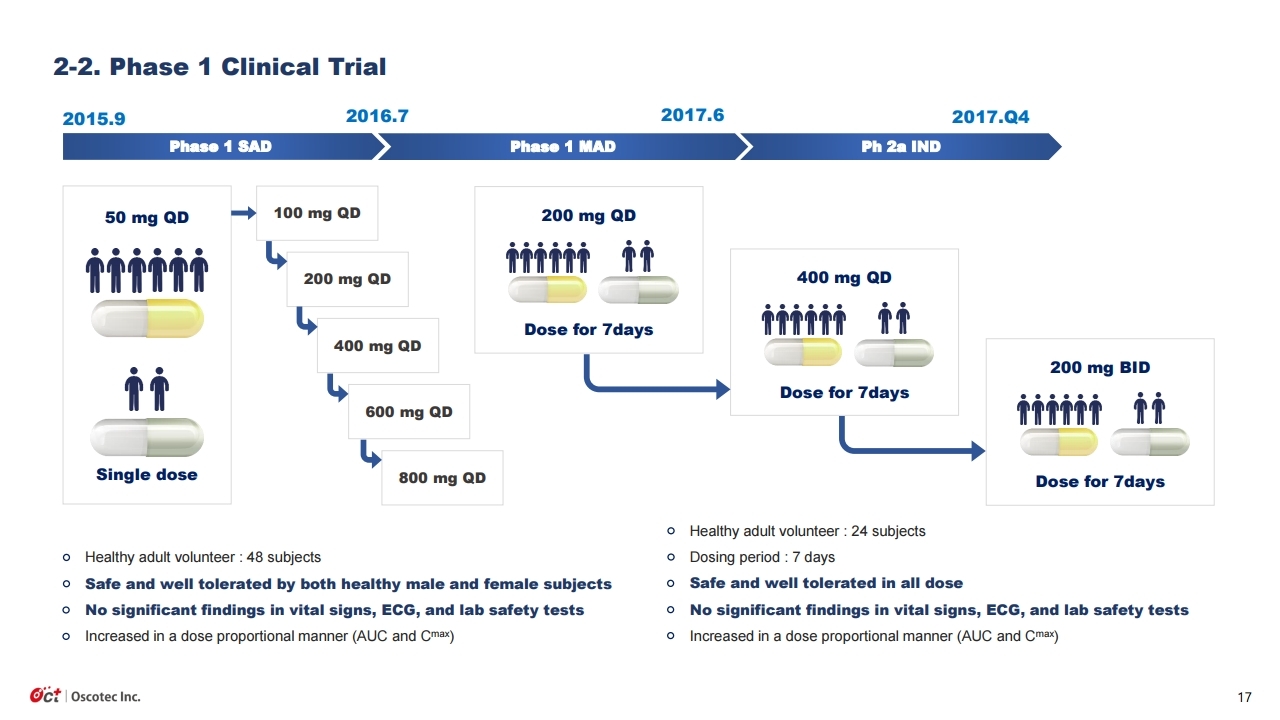
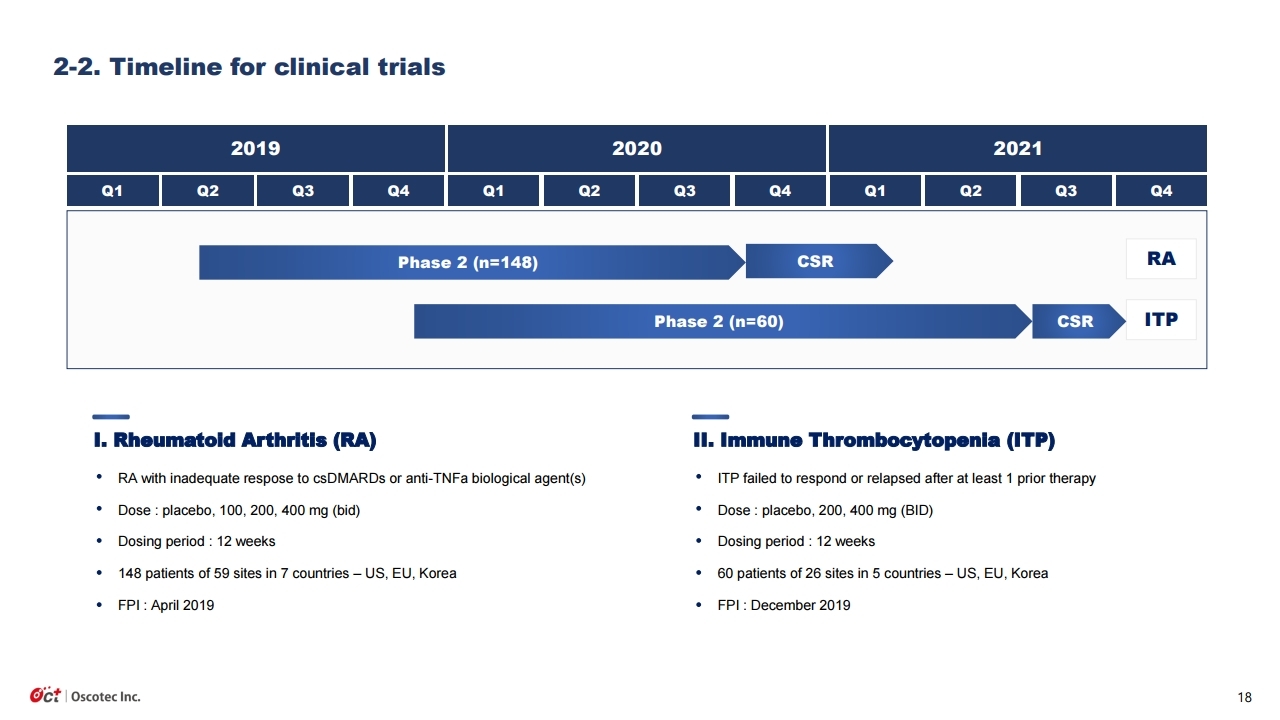
임상 결과발표라는 큰 이벤트가 끝났으나, 이게 끝이 아니고 오히려 시작이다. 연말까지 매우 많은 이벤트가 몰려 있다. 정리하면 다음과 같다. ①첫째, 10월 중 ‘레이저티닙+아미반타맙’의 글로벌 임 상 3상 투약이 시작된다. 1,000명을 대상으로 한 대규모 임상이며, 경쟁 약인 ‘타그리소’와의 직접 비교 임상이다. ②둘째, 4분기 중 얀센으로부터 레이저티닙 2차 마일스톤 수령이 예상된다. 지난 1 차 마일스톤인 3,500만불보다 훨씬 큰 6,000만불 이상이 될 것으로 예상된다. 동사는 이 중 약 40%를 수령한다. ③셋째, 올 연말 가장 큰 이벤트로 류마티스관절염 치료제 ‘SKI-O-703’ 임상 2a상의 결과발표가 예정되어 있다. 9월 투약이 종료되었으며 11월말에는 최종결과보고서를 받을 예정이다. 아무리 늦어도 내년 1월 JP모간 컨퍼런스에서는 전체 데이터가 공개될 예정이다. ④넷 째, 마지막으로 ‘레이저티닙’의 국내 조건부허가가 승인될 가능성이 있다. 유한양행은 올해 상반기 부터 ‘레이저티닙’단독투여 임상 3상을 개시하였다. 조건부허가신청은 이미 진행중일 가능성이 높 다. 매우 우수한 임상 2상 데이터가 있으며, 타그리소보다 약가가 저렴한 장점도 있다. 유사 약인 ‘올리타’의 조건부허가 사례도 있다. 식약처 입장에서 허가하지 않을 이유가 별로 없어 보인다. 연 말까지 ‘레이저티닙’의 세계최초 출시를 기대해 본다.
출처 : 한양증권 애널리스트 리포트
'기업IR 자료' 카테고리의 다른 글
| SBI핀테크솔루션즈 - 20.10.14일 기업설명회 IR자료 (0) | 2020.10.14 |
|---|---|
| 위드텍 - 독보적인 분자오염 모니터링 시스템 #10.20일 청약, 10.30일 상장 (0) | 2020.10.14 |
| 센코 - 전기화학식 센서 국산화의 주역 #상장일 10월 29일 (0) | 2020.10.13 |
| 멕아이씨에스 - 호흡치료산업을 이끄는 회사 #20.10.13일 기업설명회 IR자료 (0) | 2020.10.13 |
| 바이브컴퍼니 - 국내 AI 및 빅데이터 1위 기업 #상장일 10월 8일 #카카오 관련주 (0) | 2020.10.13 |




댓글